La tabla periódica es una de las herramientas fundamentales de la química, permitiendo la organización de los elementos en función de sus propiedades y estructura atómica. Desde su creación, ha sido clave en el desarrollo de la ciencia y la tecnología, y continúa siendo un recurso esencial en la educación y la investigación. Su estudio no solo es vital para comprender la química, sino que también tiene aplicaciones en la biología, la física, la ingeniería y la medicina.
Historia y Evolución de la Tabla Periódica
El concepto de organizar los elementos según sus propiedades químicas surgió en el siglo XIX. Entre los hitos más importantes en la historia de la tabla periódica destacan:
- 1789 – Antoine Lavoisier: Clasificó los elementos conocidos en gases, metales, no metales y tierras, sentando las bases de la clasificación química.
- 1864 – John Newlands: Propuso la ley de las octavas, observando que las propiedades químicas de los elementos se repetían cada ocho elementos.
- 1869 – Dmitri Mendeléyev: Organizó los elementos en función de su masa atómica y predijo la existencia de elementos aún no descubiertos, estableciendo la base de la tabla periódica moderna.
- 1913 – Henry Moseley: Descubrió que el número atómico, en lugar de la masa atómica, era el criterio correcto para organizar los elementos, dando lugar a la versión moderna de la tabla periódica.
Estructura y Organización de la Tabla Periódica
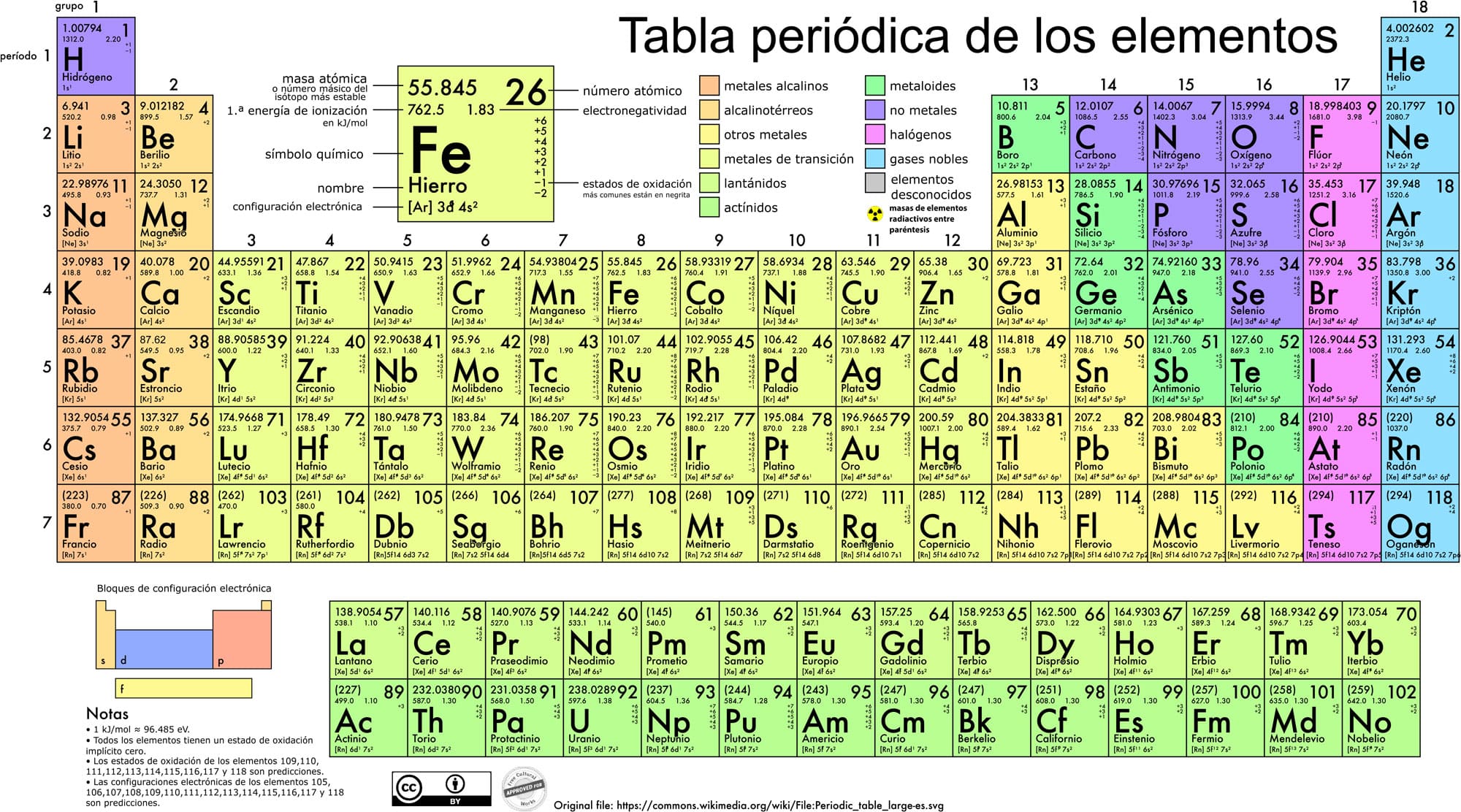
La tabla periódica actual se basa en el número atómico de los elementos y está organizada en:
- Grupos (columnas): Elementos con propiedades similares debido a la cantidad de electrones en su última capa.
- Períodos (filas): Elementos organizados según el número de niveles de energía que poseen.
- Bloques: División basada en la configuración electrónica en bloques s, p, d y f.
- Metales, no metales y metaloides: Clasificación que determina la conductividad, ductilidad y reactividad química de los elementos.
Importancia de la Tabla Periódica en la Ciencia Moderna
El impacto de la tabla periódica se extiende a múltiples áreas de la ciencia:
- Química y Física: Permite predecir propiedades químicas, reactividad y enlaces entre los elementos.
- Medicina: Uso de elementos como el carbono en fármacos, el radio en tratamientos de radioterapia y el litio en tratamientos psiquiátricos.
- Energía y Tecnología: Elementos como el uranio en energía nuclear y el silicio en la fabricación de semiconductores.
- Industria y Materiales: Aplicaciones del hierro y el aluminio en construcción, del oro y el platino en electrónica y de los gases nobles en iluminación y refrigeración.
Descubrimientos Recientes y Futuro de la Tabla Periódica
Desde el siglo XX, la tabla periódica ha seguido expandiéndose con el descubrimiento de elementos sintéticos como el neptunio y el plutonio. En las últimas décadas, se han añadido elementos superpesados como el oganesón (Og), que desafían los límites de la estabilidad nuclear y abren nuevas posibilidades en la investigación de materiales y física teórica.
Conclusión
La tabla periódica no solo es un recurso educativo esencial, sino que también es una herramienta viva que sigue evolucionando con el avance del conocimiento científico. Su estudio es clave para entender la naturaleza de los elementos y su impacto en el mundo moderno. En el futuro, seguirá desempeñando un papel crucial en la exploración de nuevos materiales, la nanotecnología y la investigación de fenómenos físicos aún desconocidos.











